Химия. 11 класс
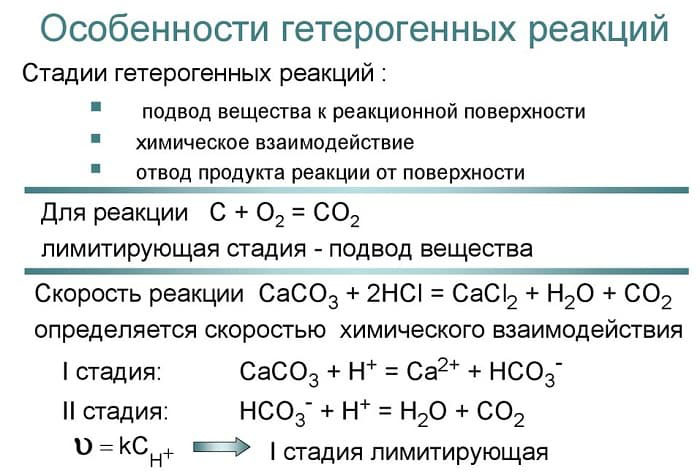
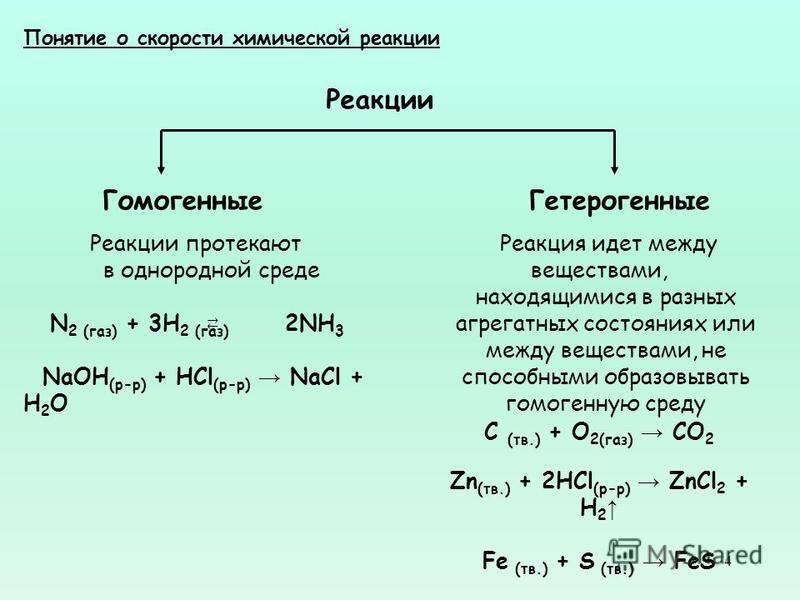
Пока что для простоты рассматривались гомогенные реакции, то есть реакции, которые протекают в однородной среде , например, в смеси газов или в растворе. Но существует множество гетерогенных процессов, идущих на поверхности соприкосновения :. Скорость гетерогенной реакции прямо пропорциональна площади поверхности соприкосновения реагентов. Например, уголь для приготовления пороха растирают в порошок. Жидкость для реакции с газом распыляют в мельчайшие капельки: так, дизельное топливо смесь углеводородов впрыскивают в камеру, где оно встречается с воздухом, через специальное устройство, обеспечивающее распыление.


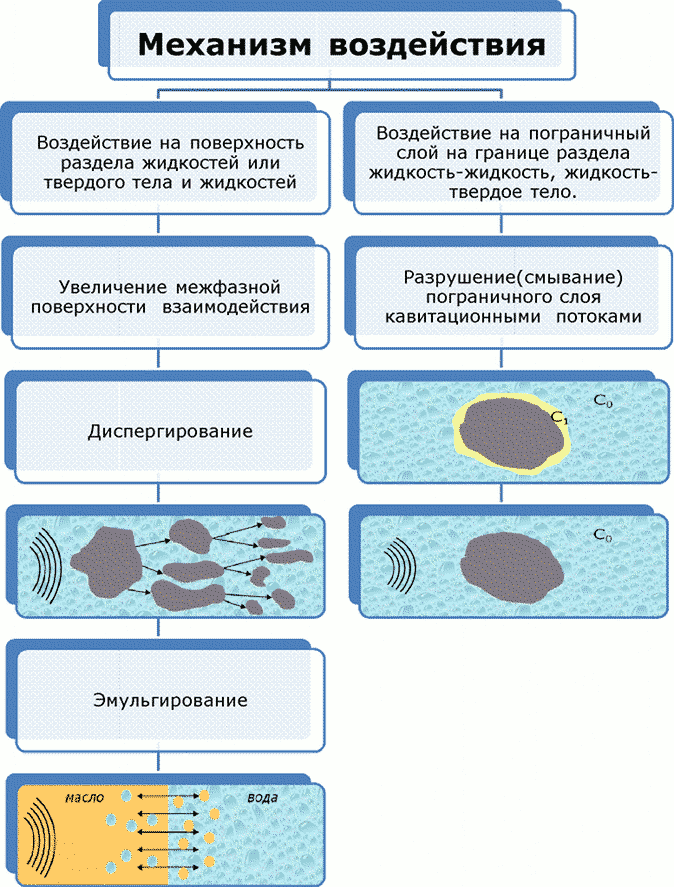

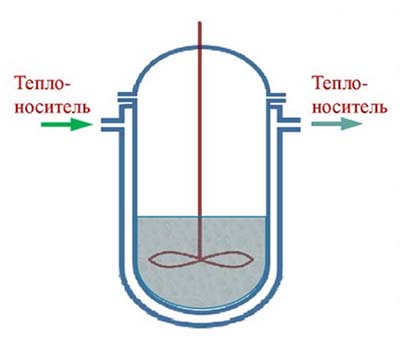



Площадь поверхности соприкосновения реагирующих веществ. На скорость гетерогенных реакций сильное влияние оказывает величина площади поверхности соприкосновения реагентов. Проведём два эксперимента и убедимся в этом. Для этого в две пробирки нальём разбавленную соляную кислоту равных объёмов.
- Гетерогенные реакции , хим. В особый класс выделяют гетерогенно-каталитические реакции, протекающие на поверхности катализатора , при этом реагенты и продукты могут и не находиться в разных фазах.
- Здравствуйте, Михаил Валерьевич. Я закончил МГУ 8 лет назад и сейчас преподаю химию школьникам.
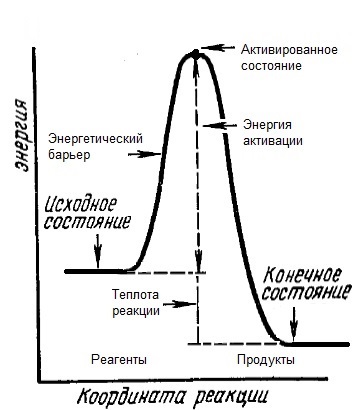
- Некоторые химические реакции происходят практически мгновенно взрыв кислородно-водородной смеси, реакции ионного обмена в водном растворе , вторые — быстро горение веществ, взаимодействие цинка с кислотой , третьи — медленно ржавление железа, гниение органических остатков. Известны настолько медленные реакции, что человек их просто не может заметить.








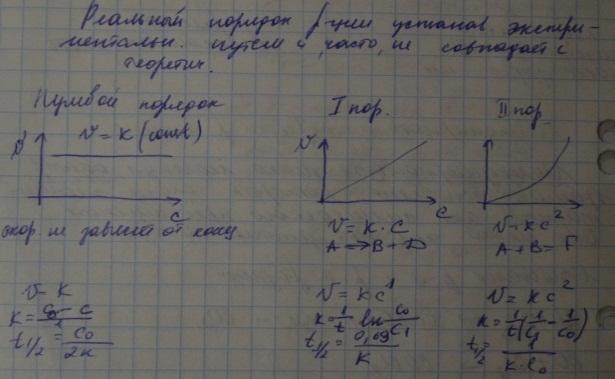
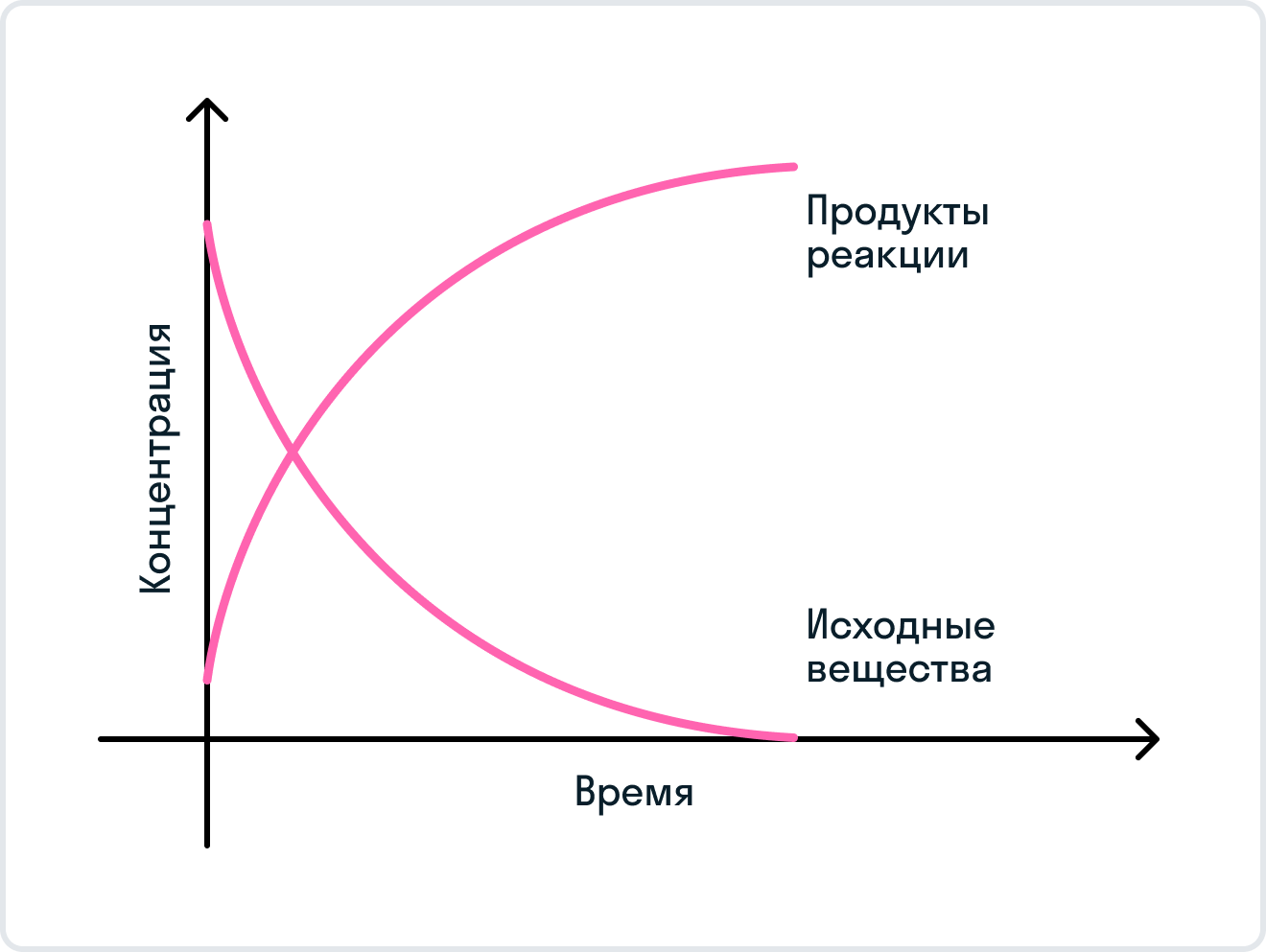
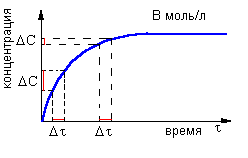
Раздел химии, изучающий изменение химических систем во времени, называется химической кинетикой. В гомогенных однородных системах в растворе или в газовой фазе скорость химической реакции определяется изменением молярной концентрации одного из реагирующих веществ в единицу времени:. Если в реакции участвует несколько веществ, то скорость можно выражать через концентрацию любого из них, так как концентрации остальных веществ связаны с ней стехиометрическими соотношениями. Согласно теории столкновений , химические реакции происходят при столкновении молекул реагирующих веществ. Поэтому скорость реакции зависит от числа столкновений и, кроме того, определяется вероятностью того, что столкновения приведут к превращению. Число столкновений определяется концентрациями реагирующих веществ, а вероятность реакции — энергией сталкивающихся молекул.